Implante subdérmico de etonogestrel en una población adolescente santafesina
Subdermal implant of etonogestrel in an adolescent population of the province of Santa Fe
Trabajo Original Dra. María Gabriela Ragogna*
Objetivo
El implante subdérmico (IS) es una de las opciones anticonceptivas reversibles a largo plazo más efectivas para adolescentes. Este estudio tuvo como objetivo evaluar la aceptabilidad y los efectos secundarios entre los adolescentes durante un año después de la colocación del IS.
Material y Método: Estudio longitudinal, prospectivo, descriptivo y observacional. Se incluyeron doscientas treinta adolescentes (230), entre 13-20 años, a las cuales se le colocó el implante de Etonorgestrel en el consultorio de Ginecología infanto juvenil del Hospital de Niños “Dr. O. Alassia” de la ciudad de Santa Fe. Las pacientes fueron citadas a control a los 3, 6, 9 y 12 meses post inserción. Se observó el patrón menstrual, peso (BMI) y los efectos adversos en cada consulta.
Resultados: Solo 113 pacientes de las 230 iniciales cumplieron los criterios de inclusión del estudio. Al momento de inserción, 72% pacientes eran nuligestas. Antes de la inserción 66% y 15% de las pacientes presentaban ritmo regular e irregular, 15% amenorrea por lactancia, y 4% no conocía el patrón menstrual. Al cabo de 1 año de control trimestral efectivo sobre 96 pacientes, 76% presentó amenorrea, 17% sangrado infrecuente, 3% sangrado frecuente, 2% sangrado prolongado y 2% ritmo regular. Un año posterior a la colocación el 7% de las pacientes refirió aumentó de mastalgia. El incremento del acné fue en un 15% y cefalea en el 6%. No se observó variaciones en el IMC. Se realizó extracción del IS en el 4,3% por sangrado, cefalea o cambio de pareja. El nivel de satisfacción del IS fue del 8,4 4 (IC95%: 8.0-8.7; escale 1-10)
Conclusión: El IS es un método con alta satisfacción por parte de la usuaria y bajo índice de discontinuación. Los efectos adversos fueron leves y bien tolerados. La amenorrea fue el patrón de sangrado más frecuente al año post inserción. Es fundamental la consejería y acompañamiento en pacientes adolescentes.
Palabras Claves: Implante Subdérmico. Anticoncepción. Adolescentes. Aceptabilidad. Efectos adversos.
ABSTRACT
Study objective: Subdermal implant (IS) is one of the most effective long-term reversible contraceptive options for adolescents. This study aimed to assess acceptability and side effects among adolescent during one year after insertion of the contraceptive device.
Material and Methods: We designed a prospective, longitudinal, descriptive and observational study. Two hundred and thirty adolescents were inserted subdermically with etonogestrel-releasing implant at Consultorio de Ginecologia Infanto-Juvenil, Hospital de Niños “Dr O. Alassia”, Santa Fe, Argentina. Patients were advised to do follow-up visits at 3, 6, 9 and 12 months post insertion. Menstrual pattern, body mass index (BMI), and side-effects were recorded at every visit.
Results: Only 113 out of 230 patients met the inclusion criteria for the study. At the time of insertion, 72% of women were nulliparas. Before implantation, 66% and 15% of the patients had regular menstrual and irregular menstrual cycles, respectively. Meanwhile, lactational amenorrhea was reported in 15% of the adolescents and the menstrual pattern was unknown in 4% of the subjects. Of the 96 patients who completed the quarterly follow-up visit schedule, 76% had amenorrhea, 17% had infrequent bleeding, 3% had frequent bleeding, 2% sustained bleeding, and 2% had regular menstrual cycle. One-year after implantation, 7% of the patients reported increased breast pain. Increase in acne and headache was observed in 15% and 6% of the women, respectively. In contrast, changes in BMI were not observed. IS was removed in 4.3% of the subjects due to bleeding, headache or partner change. Average satisfaction level of IS users was 8.4 (IC95%: 8.0-8.7; scale 1-10)
Conclusión
IS is a method with high user satisfaction and low discontinuation rate. Adverse effects were mild and well tolerated. Amenorrhea was the most frequent bleeding pattern at one year post-insertion. Counseling and support in adolescent patients is essential to help make IS accessible to them.
Key Words: Subdermal Implant. Contraception. Adolescents. Acceptability. Side effects.
INTRODUCCIÓN
La recomendación y elección de un método anticonceptivo en adolescentes presenta desafíos especiales. No solo es importante ofrecerle un buen método anticonceptivo que evite los embarazos no deseados sino que debemos educarlos en la prevención de infecciones de transmisión sexual (ITS) y acompañarlos en el descubrimiento y ejercicio de una sexualidad placentera y responsable. Los métodos anticonceptivos en la adolescencia deben tener idealmente: eficacia, seguridad, posibles efectos beneficiosos no contraceptivos, facilidad de uso, costo accesible y reversibilidad (1).
Según ha sido demostrado en varios trabajos los anticonceptivos reversibles de acción prolongada (LARS) son más efectivos que los anticonceptivos orales, los parches transdérmicos o los anillos vaginales (2).
La Academia Americana de Pediatría en el año 2014 recomienda que a los adolescentes sexualmente activos se les ofrezca anticoncepción reversible de acción prolongada, que son altamente eficaces y no requieren acciones diarias (3) acompañados de métodos de barrera para protección de ITS. Las características de los implantes subdérmico indican que es una de las mejores opciones anticonceptivas para las adolescentes.
El implante subdérmico actualmente utilizado en Argentina contiene Etonorgestrel (ETN). El ETN es un metabolito activo del Desorgestrel se une con alta afinidad a los receptores de progesterona en los órganos blanco, se libera diariamente en el tejido subcutáneo, ofreciendo 3 años de anticoncepción. Posee una alta efectividad anticonceptiva tiene un índice de Pearl de 0,38 embarazos por cada 100 mujeres /año con uso correcto a los 3 años de su uso (4,5).
El mecanismo de acción incluye la inhibición de la ovulación, espesamiento del moco cervical, atrofia endometrial e inhibición de la capacitación espermática (6).
Entre las principales ventajas de los implantes se ha identificado la liberación estable del fármaco, independiente de la voluntad de la usuaria evitando fallas de este modo, lo que se asocia con seguridad y confianza. Pero también se han descripto efectos adversos no deseados, entre los más frecuentes, se encuentran las alteraciones del ciclo menstrual, cefalea, aumento de peso y acné (7).
En el presente trabajo se evaluaron diferentes parámetros clínicos en un grupo de adolescentes del Servicio de Ginecología Infanto Juvenil del Hospital de niños “Dr. Orlando Alassia” (HNOA) de la ciudad de Santa Fe que recibieron implantes subdérmico de Etonorgestrel.
MATERIAL Y METÓDOS:
DISEÑO DE LA INVESTIGACIÓN:
Se realizó un estudio de tipo longitudinal, prospectivo, descriptivo y observacional en una cohorte de adolescentes portadoras del Implante Subdérmino de Etonorgestrel (IS) en el consultorio de Ginecología Infanto Juvenil del HNOA de la ciudad de Santa fe, en el periodo comprendido entre Enero 2015 y Agosto 2016.
POBLACIÓN Y CRITERIOS DE INCLUSIÓN:
Del total de 230 pacientes a las cuales se les colocó el IS, se seleccionaron para el presente estudio a 113 que cumplieron un año al menos de su colocación, aceptaron por escrito ser incluidas en el estudio y cumplieron con los controles trimestrales previamente acordados. Con pérdida de 5 pacientes que solicitaron su retiro precoz en el último trimestre.
Criterios de exclusión: pacientes que no dieron su consentimiento, con acné o que no cumplían con los criterios médicos de elegibilidad según OMS (8,9).
IMPLANTE:
El IS (IMPLANON NXT) provisto por el Ministerio de Salud de la Nación, se colocó según técnica a todas las pacientes del estudio en consulta programada, con la debida certeza de que no estaban embarazadas (10,11).
EVALUACIÓN CLÍNICA Y SEGUIMIENTO A PARTIR DE LA COLOCACIÓN:
A cada paciente en su primera consulta se le realizó la historia clínica (12).
Se completó una ficha de seguimiento (antecedentes gineco-obstétricos, ritmo menstrual y métodos anticonceptivos, referencia de dismenorrea, cefalea ó acné). En el examen físico se recabaron la talla, peso, IMC y presión Arterial.
En cada consulta trimestral se procedió a chequear el implante por palpación, pesar y tallar a la paciente, observar el calendario menstrual (clasificación FIGO 2011) y evaluar la aparición clínica de acné, cefalea o mastalgia. Se resolvieron dudas, se indicó tratamiento por los sangrados en los casos necesarios y se reforzó la utilización de métodos de Barrera (13).
Al término del año de seguimiento se solicitó a las pacientes que puntuaran en una escala del 1 al 10 su satisfacción respecto al método elegido.
Los datos del momento de la inserción y sus seguimientos trimestrales por un año se recogieron en una planilla Excel, diseñada a tal fin.
ANALISIS ESTADÍSTICO:
Los análisis fueron llevados a cabo con el software IBM SPSS v 23.0. Las variables cuantitativas se expresan con medias y sus respectivos intervalos de confianza del 95%. Las variables cualitativas se expresan con porcentajes y sus correspondientes recuentos. Las comparaciones de variables numéricas entre diferentes momentos temporales se realizaron mediante pruebas t de muestra dependientes. Valores p menores a 0,05 fueron considerados estadísticamente significativos.
RESULTADOS:
Se estudiaron un total de 113 pacientes con una media de edad de 16.8 (IC 95%: 16,4-17,8). Rango de edad 13-20 años, a todas se les colocó el IS y realizaron su seguimiento en el consultorio de Ginecología Infanto Juvenil del Hospital de Niños “Dr. Orlando Alassia” de la ciudad de Santa fe.
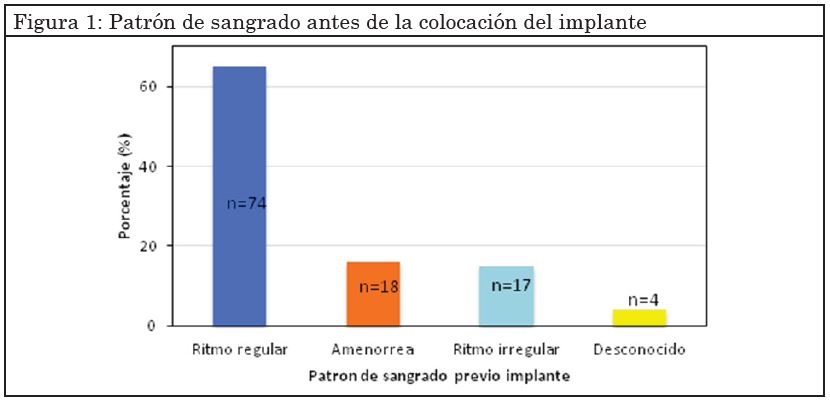
El 72% (n=82) eran nuligestas y el 28% (n=31) tenían antecedentes de 1 o 2 embarazos, la media de edad de este grupo fue de 18,5 años con IC 95%=(17,9-19,0). En las 113 pacientes estudiadas se observaron 3 patrones de sangrando previos al implante: regular, amenorrea por lactancia e irregular. La mayoría de las pacientes (65%) tenían un ritmo regular al momento de la inserción, mientras el 35% restante de las pacientes presentaban otros ritmos menstruales o lo desconocían (Fig.1)
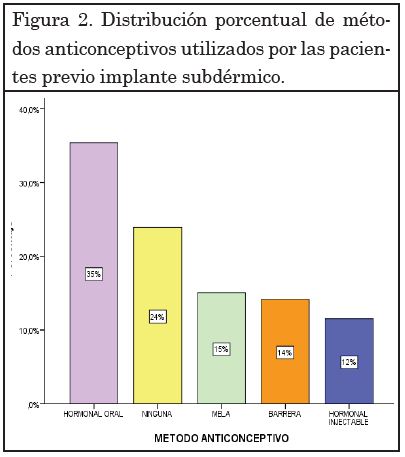
Se registró que método anticonceptivos utilizaba la adolescente y su pareja al momento de la colocación del implante. El 76% de las pacientes usaban algún método anticonceptivo mientras que el 24% de las pacientes no utilizaban ningún método de control de la natalidad (Figura 2).
Antes del inicio del tratamiento el 65% (n=74) de las pacientes no presentaban dismenorrea, el 18% (n=20) refirieron dismenorrea leve y el 17% (n=19) moderada. El 27% (n=30) de las pacientes que refirieron el síntoma pasaron de padecer dismenorrea leve-moderada a ausente al año del tratamiento. Sólo en el 8% (n=9) persistió el síntoma. El cambio de dismenorrea presente a ausente luego del año de tratamiento fue estadísticamente significativa (Test de McNemar, p<0,01).
Sólo el 24% (n=26) de las usuarias refirieron mastalgia antes de la colocación del implante. Al año el 17% (n=18) manifestaron una mejoría del síntoma, y el 7% (n=8) empeoraron su percepción de mastalgia. Tanto los cambios de disminución como de aumento de mastalgia fueron estadísticamente significativos (Test de McNemar, p<0,01).
Al inicio del tratamiento ninguna paciente presentaba acné clínico o antecedentes de tratamiento médico del mismo (criterio de exclusión). Al año se observó que un 15% (n=16) sufrieron acné.
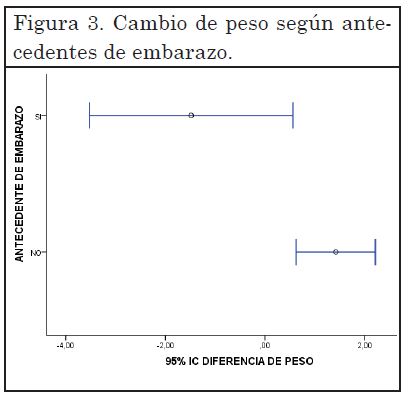
El 6% (n=7) de las pacientes sufrieron aumento de cefaleas luego de un año de tratamiento y 1% (n=1) manifestó una disminución de las mismas. El restante 93% no percibió cambios. Tanto los cambios de disminución como de aumento de cefaleas no fueron estadísticamente significativos (Test de McNemar, p>0,05). El índice de masa corporal no presentó diferencias estadísticamente significativas (p>0,05) entre las evaluación al comienzo y al año de tratamiento. Las pacientes sin antecedentes de embarazo (n=82/113) en promedio aumentaron 1,420 kg (IC 95%: 0,62-2,25) durante el año evaluado, mientras que las pacientes con antecedentes de embarazo (n=31/113) en promedio disminuyeron 1,484 kg (IC 95%: 0,55-3,52) durante el mismo periodo. (Figura 3)
El 4,3 % (n=5) solicitaron el retiro temprano del implante por sangrado (n=3) que no mejoraba con el tratamiento, cefalea de aparición brusca (n=1) y cambio de pareja (n=1).
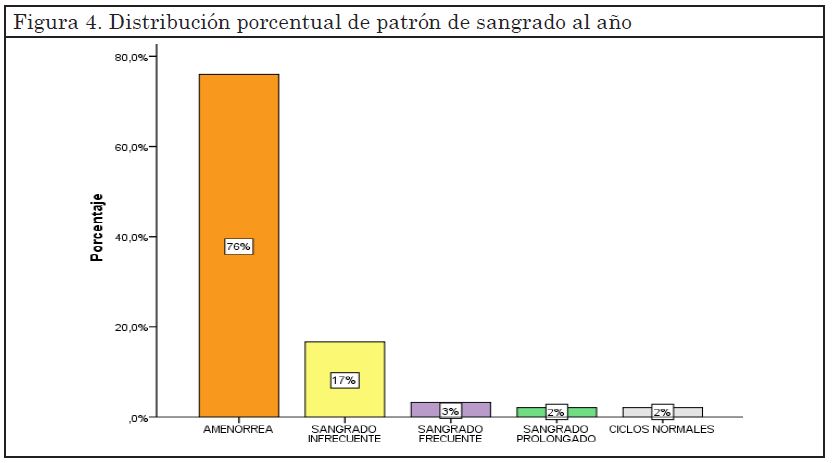
Sobre un total de 96 pacientes con seguimiento trimestral completo; al término de un año el 76% (n=73/96) presentó amenorrea al año, el 17% (n=16/96) sangrado infrecuente, 3% (n=3/96) sangrado frecuente, 2% (n=2/96) sangrado prolongado y el 2% (2/96) ritmo regular. (Figura 4)
El 76% (n=56/96) de las pacientes que presentaron amenorrea al año de control, eran pacientes que antes de la colocación del implante presentaban amenorrea por lactancia (n=18/96) o hipomenorreas por estar con régimen anticonceptivo hormonal (n=38/96).
En la observación trimestral en el 40% (n=38) de las pacientes hubo un cambio entre el patrón de sangrado del primer trimestre y el cuarto trimestre, siendo el cambio más frecuente (n=25) el de sangrado infrecuente a amenorreas.
Durante el año 32 pacientes presentaron sangrado frecuente o prolongado que fueron tratadas con drogas antiinflamatorias en el 66% (n=21/32) y con esquemas hormonales en un 34% (n=11/32).
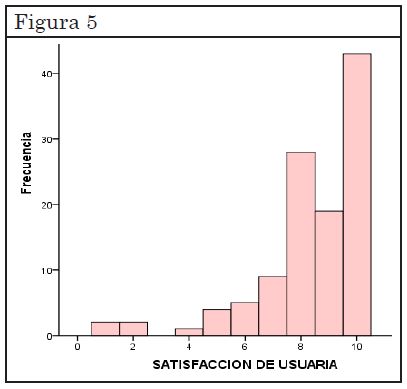
La variable satisfacción de usuaria mostró una media de 8,4 (IC 95%: 8,0-8,7) y una mediana igual a 9. (Figura 5)
En la muestra evaluada a un año no hubo embarazos.
DISCUSIÓN:
En el presente estudio evaluamos los efectos secundarios, efectividad y aceptabilidad del implante subdérmico de Etonogestrel colocado en una población de jóvenes menores de 21 años. A pesar de sus ventajas, existe poca información respecto a sus efectos en población adolescente ya que las mayorías de los estudios se han realizado en mujeres de 18 a 40 años de edad (8, 14).
En la cohorte evaluada, 39/113 (35%) de las pacientes presentaban dismenorrea leve o moderada al comienzo del estudio mientras que al completar el año de implante solo 8/113 (7%) de las adolescentes persistieron con el síntoma. A diferencia de nuestro hallazgos, la encuesta realizada por SAGIJ a 1477 adolescentes que concurrieron a consultorios mostro que el 58.9% de ellas presentaban dismenorrea (15).
Pueden existir varias razones que expliquen las diferencias observadas en el registro del síntoma entre diferentes estudios, según cómo se realice el interrogatorio, la naturalización social de la misma y la percepción subjetiva; esto incrementa las chances de variabilidad en el registro de este síntoma entre diferentes estudios.
Por otra parte, una elevado número de pacientes en nuestros estudio utilizaba anticonceptivos hormonales previo al implante 47% (n=53/113). Uno de los efectos principales no contraceptivo de los anticonceptivos hormonales es la disminución de la dismenorrea (debido a sus acciones anovulatorias, hipoplasia endometrial, menor flujo menstrual y prostaglandinas (16)). Otra posible explicación del menor porcentaje de pacientes con dismenorreas es que un gran porcentaje de pacientes eran adolescentes de temprana edad (10-14 años), que probablemente aún no la presentaban. Por último, es importante notar que el 15 % (n=18/113) de las pacientes evaluadas en nuestro servicio presentaban amenorrea por lactancia, lo que incremento sensiblemente el número de pacientes sin síntoma de dismenorrea al momento de la inserción del implante.
Al igual que otros investigadores observamos una disminución del 80% de dismenorrea post inserción del implante (17,18). Este cambio está asociado a la supresión de la ovulación y reducción del tejido endometrial inducido por el Etonorgestrel que causa i) amenorrea y ii) aumento de la progesterona que inhibe la síntesis de prostaglandinas y Leucotrienos endometriales que son mediadores del dolor menstrual (15, 16, 19). Aunque los resultados de nuestra investigación y la de otros colegas indicarían que el implante subdérmico es una buena opción para el tratamiento de la dismenorrea, no existe todavía evidencias sólidas para hacer ese tipo de recomendación. Es por ello que para el National Institute for Health and Care Excellence (NICE), el implante subdérmico es una recomendación clase C para el tratamiento de la dismenorrea (10).
El 76% de las pacientes no referían mastalgia previo al implante ni tampoco manifestaron mastodinia al cumplirse el año del implante. Existen diferentes razones que explicarían el alto porcentaje de pacientes sin mastalgia en nuestro estudio previo implante. Aunque la mastalgia es un motivo de consulta en la adolescencia, es un síntoma que no se presenta en muchas pacientes. Nuestra población era heterogénea al inicio del estudio, aproximadamente el 47 % (n=53/113) de las pacientes utilizaban anticonceptivos hormonales de bajas dosis o inyectables y un 15% (n=18/113) estaba en amenorrea por lactancia; por lo tanto el 62 % no presentaban mastodinia probablemente por estar bajo tratamiento hormonal o simplemente por estar amamantando al momento de la entrevista.
Antes de la colocación del implantes, sólo el 24% (n=26/113) de las usuarias refirieron padecer mastalgia. Al año, 18 de las mismas refirieron una mejoría del síntoma mientras que 7% (n= 8) pacientes empeoraron la percepción del mismo.
Existen dos mecanismos fisiopatológicos que explican la presencia de mastodinia: el primero es el desbalance estrógeno progesterona que ocasiona un crecimiento irregular entre estroma, conductos y lobulillos dando la hipersensibilidad y turgencia mamaria. El segundo tipo de dolor es la mastodinia aguda que acompaña a los cuadros de distress, donde se produce un aumento de la liberación de prolactina, esto interfiere en la producción de GnRH y altera la relación estrógeno/progesterona además de incrementar la formación de receptores de estrógenos en la mama (15).
El Dr. Fraser realizó una revisión de 11 estudios internacionales (n=940 mujeres) sobre implante subdérmico, llegando a la conclusión que la aparición de mastodinia o su aumento como efecto adverso fue de 10,2 % (14). El número de la muestra del presente trabajo es pequeño para compararla con otros estudios pero podríamos inferir que las pacientes portadoras del implante que al inicio refirieron mastodinia (n=26/113), al presentar amenorrea, con un ambiente hormonal constante sin fluctuaciones, sin disbalance cíclico en 18 de ellas se observó mejoría. Además debemos considerar que durante las observaciones trimestrales, si las pacientes manifestaban dolor mamario, se realizaban intervenciones médicas en cuanto a la corrección de dietas ricas en metilxantinas (sustancias, en discusión actualmente, que podrían producir mastalgias), el uso de sostén adecuado y eventual medicación con AINES. Respecto al 7% (n=8/113) de aumento en la percepción podría deberse al efecto adverso descripto para el implante o tal vez podría tratarse de pacientes con distress en el momento de la última observación. Tanto los cambios de disminución como de aumento de mastalgia fueron estadísticamente significativos (Test de McNemar, p<0,01), para nuestra muestra y es solo un poco menor que para el resto de los estudios (14).
Un criterio de exclusión en el presente estudio fue que al inicio del tratamiento ninguna paciente presentara acné clínico o antecedentes de tratamiento médico del mismo. Los gestágenos de tercera generación como el anticonceptivo hormonal del implante (Etonogestrel, su metabolito) tienen un leve efecto androgénico, que puede inducir el desarrollo de acné. Sin embargo en la “National clinical guide clearhouseing de USA” (CEU GUIDE) 2014, advierte que la mujer que utiliza implante subdérmico puede mejorar, empeorar o no tener cambios del acné durante su uso (10). En nuestro trabajo se observaron dos patrones, el 85% de los pacientes no presento cambios dermatológicos mientras que un 15% de las adolescentes desarrollaron acné. En concordancia con nuestros hallazgos, Blummenthal y colaboradores también reportaron que el 15% de las pacientes que no tenían acné lo presentaron durante el tratamiento anticonceptivo y además que en el 14% que inicialmente tenía acné se observó un aumento de la severidad del mismo (20). Una confirmación de estas observaciones es el trabajo de Fraser que informo que el 18,4% de los pacientes examinados presentaban el acné como efecto adverso (14). Un trabajo realizado en Asia en 110 mujeres puérperas y nulíparas encontraron una incidencia del 15,3% de acné a predominio de las pacientes sin antecedentes obstétricos (21). Las pacientes con acné incluidas en nuestro estudio se las trató con medidas locales y antibióticos según el caso. Es importante remarcar que este efecto adverso no motivó a las pacientes en nuestros estudio a solicitar el retiro del implante.
De 113 pacientes que iniciaron el tratamiento solo 7 manifestaron aumento de cefalea y sólo una refirió disminución de las mismas, el resto no presentó cambios. La cefalea es un síntoma general, puede estar asociada al ciclo menstrual y ser un componente del síndrome disfórico premenstrual; por lo tanto se ve beneficiada por la anticoncepción hormonal ya que con esta se evita las fluctuaciones séricas de estradiol o progesterona. Por lo tanto, que la mayoría de los pacientes no hayan presentado cefaleas después del implante subdérmico es esperable teniendo en cuenta la acción farmacológica asociado a los anticonceptivos hormonales descriptos previamente. En nuestro estudio solo el 6% (7/113) de los pacientes presentaron cefaleas durante el año control. Otros investigadores observaron que la cefalea estuvo presente entre el 12,5% y 15,3% de las pacientes con implante subdérmico (14, 20, 21,22). No existe evidencia que la progesterona induzca la cefalea (10). Por lo tanto los casos reportados aquí y en otros estudios pueden deberse a otras causas, que no tienen relación con la hormona incluida en el implante, como serían las cefaleas de origen tensional. No podemos, de todas maneras, descartar que algunas de las pacientes podrían haber sufrido de cefaleas o migrañas de origen vascular antes del implante y no haberlo reportado y que hayan experimentado un recrudecimiento del dolor de cabeza que si está asociado a la progestina liberada por el implante subdérmico (10).
En la primera evaluación de los datos con respecto al peso pudimos observar que no hubo cambios significativos del mismo al cabo del año de seguimiento, ante tal evidencia no concordante con la bibliografía hicimos una nueva revisión separando a aquellas pacientes que estaban en periodo de lactancia o puerperio sin lactancia (n=31/113) recuperando su peso. Allí pudimos observar dos comportamientos claros; de las lactantes o puérperas sin lactancia que tuvieron un promedio de descenso de peso de 1,500 kg a lo largo del año control y el otro grupo, nulíparas (n=82/113) que presentó un aumento de 1,500 kg/año. Incide en este resultado el hecho de control de peso trimestral a las pacientes, lo cual nos dio la oportunidad de corregir los hábitos, indicar dieta y actividades físicas a las mismas según el peso encontrado. El Dr. Blumenthal reportó que el 31% de las pacientes no experimentaban cambios en su peso e inclusive algunas perdían peso, 25 % aumentó hasta 2,5 kg, 24% desde 2,5 a 5 kg, 9% un incremento de 5 a 7,5 Kg y el otro 11% más de 7.5 kg, pero en este trabajo solo se evaluó el peso al año de la colocación del método (19). Este trabajo sobre 940 pacientes no tenía seguimiento trimestral y por lo tanto no pudieron intervenir en la observación temprana del aumento de peso como lo hicimos nosotros. En conclusión en nuestra muestra el índice de masa corporal no presentó diferencias estadísticamente significativas (p>0,05) entre las evaluación al comienzo y al año de tratamiento.
Al término del año post implante, de las 96 pacientes con seguimiento trimestral completo, el 76% (n=73/96) presentó amenorrea, el 17% (n=16/96) sangrado infrecuente, 3% (n=3/96) sangrado frecuente, 2% (n=2/96) sangrado prolongado y el 2% (2/96) ritmo regular. Esta variabilidad en el patrón de sangrado asociado al uso del implante subdérmico ya ha sido observado con anterioridad por otros investigadores (8). Esos cambios, que son impredecibles, pueden ser en frecuencia (ausencia, menor o mayor frecuencia o continuo), en intensidad (aumentada o disminuida) o en duración (8).
En las pacientes usuarias de implante se produce la liberación de Etonorgestrel, el cual induce una supresión uniforme de la proliferación endometrial, independientemente de la fase del ciclo menstrual. La intensa supresión endometrial se traduce en una reducción en la cantidad y duración del sangrado menstrual hasta la aparición de amenorrea (8,20).
Estos cambios fisiológicos inducidos farmacológicamente explican el alto porcentaje (76%) de pacientes en nuestro estudio que presentaron amenorrea al cabo de un año de uso del implante subdérmico. Sin embargo otros investigadores reportaron, en contraposición con nuestros hallazgos, tasas menores de amenorrea que variaron entre el 17,4% al 22% (4, 8, 23,24).
Esta diferencia nos obligó a analizar el perfil de nuestro cohorte, observando que de las 73 pacientes que presentaron amenorrea al cabo de un año de la colocación del implante, 53 de ellas previo al implante ya presentaban ciclos regulares con escaso sangrado menstrual (hipomenorrea) por la ingesta de anticonceptivos de bajas dosis hormonales y otras 18 pacientes presentaban amenorrea por lactancia al momento de la colocación. A partir de nuestro análisis es válido especular que sobre un endometrio de espesor disminuido por la exposición a bajas concentraciones de estrógenos, la colocación de un implante subdérmico con Etonorgestrel puede inducir con mayor rapidez y eficacia atrofia endometrial y en consecuencia amenorrea.
Observamos también en nuestro estudio que un porcentaje de mujeres presentaban patrones de sangrado irregular luego de la colocación del implante. El mecanismo y los factores que determinan la aparición de episodios de sangrado irregular en usuarias de implantes no están totalmente aclarados, habiéndose planteado diferentes causas etiológicas: aumento de la densidad microvascular, atrofia endometrial, disminución de la expresión de la tromboplastina y endotelina, aumento de la fragilidad vascular o la expresión anómala de las metaloproteinasas de la matriz extracelular (MMP). En general todos los mecanismos previamente citados conducen a una mayor fragilidad vascular endometrial y, como consecuencia, a la aparición de sangrado irregular (33).
La importancia de este tipo de alteraciones del patrón de sangrado radica en que son responsables de un alto porcentaje, entre 40 y 70% del abandono del método o retiro precoz (1,9, 15,22, 23).
El sangrado frecuente o prologando no afecta la salud de la paciente pero puede interferir en la realización de actividades diarias, disminuyendo el bienestar general. Durante el año de control el 33% (n=32/96) de las pacientes sufrieron sangrado frecuente o prolongado a las cuales se las acompañó, observó y trató oportunamente con anti inflamatorios no esteroides (AINES, 500 mg cada 8 hs por 5 días), antifibrinolítico (Ac. Tranexámico 500 cada 8 por 3-5 días) y en tercera línea anticonceptivos con 30 EE más LNG por al menos dos ciclos, siguiendo las recomendaciones del Centro de Control y Prevención de enfermedades (CDC) en su guía de recomendaciones para el uso de anticonceptivos 2013 (11). De las 32 pacientes que recibieron tratamiento médico, sólo 5 persistieron con el síntoma, presentando sangrado frecuente 3/32 y sangrado prologado 2/32 al término del año control. Al término del cuarto trimestre 3/32 de ellas solicitaron el retiro precoz por la molestia que les generaba el sangrado no resuelto. Por lo expresado es importante disponer de un tratamiento efectivo del sangrado irregular durante el uso de gestágenos solos, ya que reduce la tasa de abandono por este efecto secundario. Conocida la etiología del sangrado irregular, descartando previamente lesiones orgánicas, la medida que puede resultar más efectiva es la información previa y adecuada, lo cual se llevó a cabo en los encuentros de consejería, de forma que la mujer conozca la posibilidad de su aparición y esto no genere una situación de estrés que conduzca al abandono del método. Hasta la fecha se han probado varios y diferentes tratamientos para el sangrado irregular en mujeres usuarias de gestágenos. La principal limitación de los tratamientos experimentados (antiinflamatorios no esteroides, norestisterona, anticonceptivos, doxiclina e incluso tamoxifeno) es que aunque la mayoría son capaces de reducir la duración de los episodios de sangrado no se obtienen buenos resultados a largo plazo (25, 26,33). Resumiendo, en nuestro estudio, el 84 % (27/32) de las pacientes resolvieron su sangrado con el tratamiento indicado. Altas tasas de resolución del sangrado también han sido publicados por otros colegas que utilizaron tratamientos hormonales en mujeres con sangrado frecuente o prolongado por el uso de implante (27, 28).
En el presente trabajo la tasa de discontinuidad de IS fue sólo el 4,3% (n=5/113), 3 pacientes solicitaron el retiro por sangrado prolongado o frecuente, 1 por cefalea de aparición brusca en estudio y 1 paciente por cambio de pareja.
En la revisión bibliográfica encontramos una tasa de discontinuidad antes de los doce meses de inserción que oscila alrededor del 18% -32% (9,14, 23, 27, 28, 29, 30,31).
Diferentes estudios muestran que la tasa de discontinuidad antes de los doce meses de inserción oscila entre el 10,3% al 19% en adolescentes (29, 23) y entre 18% -32% (20, 27) en mujeres mayores de 18 años. En el presente trabajo la tasa de discontinuidad de IS fue sólo el 4,3% (n=5/113). Al igual que lo observado en nuestra investigación, otros colegas han reportado que la principal causa para discontinuar el uso del implante tanto en adolescentes como adultos son los sangrados prolongados y frecuentes (1, 13, 14, 17, 24, 30, 31,33).
Es importante remarcar que no se han detectado diferencias significativas entre las poblaciones de adultas o adolescentes que solicitaron remoción (15, 16, 30, 31,33) por esta causa. Estos estudios parecen sugerir que el sangrado en las adolescentes no es un factor de riesgo para la discontinuidad del método (28, 29,30).
Estimamos que la baja tasa de discontinuidad en el uso del implante observado en nuestro grupo fue debido principalmente a una educación previa de las pacientes, que redundo en una mejor tolerancia al cambio del sangrado menstrual y una mayor adherencia al método anticonceptivos recomendado. Otro factor que puedo haber incidido en la baja tasa de discontinuidad es que aquellas pacientes que tuvieron sangrado frecuente o prolongado se les indicó tratamiento terapéutico, que resolvió favorablemente el cuadro hemorrágico en la gran mayoría de los casos, evitando así la extracción temprana del implante. Desafortunadamente no estamos en posición de comparar estos aspectos de nuestro estudio respecto a investigaciones similares ya que en estas últimas no existe información concreta si los retiros por sangrado habían recibido o no algún tipo de tratamiento o consejería médica adecuada (8, 27).
El punto clave para una buena tolerancia de los cambios del patrón menstrual, los efectos adversos y una baja tasa de discontinuidad es la consejería médica adecuada.
La satisfacción de la usuaria fue alta para nuestra población (mediana igual a 9). Para la Dra. Obijuri la satisfacción en un grupo de adolescentes de similares características al estudiado fue del 60-70% (22).
En nuestra experiencia pudimos observar los buenos resultados, la tolerabilidad a los efectos adversos y la satisfacción de la usuaria a un año de su colocación, en función de una minuciosa educación previa. Citar a la paciente las veces que sea necesario, explicar verbalmente y por escrito el procedimiento, el mecanismo de acción, la durabilidad, y los efectos sobre el patrón menstrual dan como resultado una mejor aceptación, adherencia al método y tolerabilidad ante los efectos secundarios que pudieran aparecer. Estos encuentros son enriquecedores para el equipo de salud porque permite escuchar al otro, saber cuáles son los mitos, fantasías sociales que pueden eventualmente entorpecer la aceptación o continuidad de cualquier método.
La educación en prevención de ITS fue constante y activa en los distintos encuentros previos a la colocación y en el seguimiento posterior, ya que pudimos evidenciar que sólo el 14% (n=16) de los adolescentes utilizaban preservativos siendo sexualmente activos al momento de la consulta. A la vez observamos que el 24% (n=27) de las adolescentes no estaban utilizando ningún método anticonceptivo lo que nos lleva a asegurar que a pesar de existir grandes fuentes de información no se traduce necesariamente en una educación sexual responsable en escuelas y hogares.
CONCLUSIONES:
En este trabajo la amenorrea fue el patrón menstrual más frecuente al año de inserción.
Los sangrados frecuentes o prolongados fueron tratados exitosamente con medicación oral y solo fue motivo de discontinuación en un 3% de las pacientes tratadas.
Se registró alta satisfacción y bajo índice de discontinuidad, los efectos adversos no relacionados con la menstruación fueron leves y tolerables.
La presencia de efectos secundarios no influye en la utilización y recomendación del implante como método anticonceptivo, relacionado con las características de ser seguro, eficaz, accesible, cómodo, discreto, temporal de larga duración, práctico, las cuales son más importantes para las usuarias que la presencia de los efectos secundarios.
Se advirtió baja utilización de métodos de barrera para una población de riesgo sexualmente activa al momento de la consulta. Es fundamental la consejería y el acompañamiento en el uso del IS y la prevención de ITS. Se deberá continuar el registro de portadoras de IS para generar mayor certeza sobre los datos obtenidos.
AGRADECIMIENTOS: Dra. Estela Curá y Dra. María C. Fábrica por su colaboración en la colocación, seguimiento y recolección de datos.
BIBLIOGRAFÍA
- Castillo A; Moriena M y col. “Elección de métodos anticonceptivos y frecuencia de uso de implantes subdérmico en adolescentes que concurrieron al consultorio de adolescencia del Hospital Lucini, provincia de Córdoba a, entre enero y julio 2015”. Revista AMADA 2016. Vol. 14-n°1; 14-24.
- Winner B, Peiper JF y col. “Effectiveness of long-acting reversible contraception” The New England J of Medicine 2012; 336(21): 1998-2007.
- http://wwwmpr.r/section/health-shots/2018/08/31/492101014 drop-in-teen-pregnancies-is-ane-to-more-contraception-not-less-sex?
- Trunsell. J contraceptive failure in the United States. Contraception 2011; 83:397-404.
- Hohmann H. Examiniting of efficiency, safety and patient acceptability of Etonorgestrel implantable contraceptive. Patient preference and adherence 2009; 3: 205-211
- Orzerovich S; Labosvsky M. “Anticoncepción de larga duración en la adolescencia”. Ginecología Infantojuvenil, un abordaje interdisciplinario. Ed journal 2014. Cap. 10.6:597-620.
- Patiño A; Ruelas MC et al. “Evolución a un año de los efectos adversos, en una cohorte de pacientes con implnate subdérimco de desogestrel”. Rev Chilena de Obstetricia y Ginecología 2006, vol71, n.3.
- Mansoru D, Korver T, et al. The effects of implanon on menstrual bleeding patterns. Eur J Contracept Reprod Health Care 2008; 13 (Suppl 1):13-28.
- CDC US medical eligibility criteria for contraceptive use, 2016. http:/www.cdc.gov/repreductivehealth/unintendedpregnancy/USMEhtm
- Progeston-only implants. 2014. National Guideline Clearinghouse, Agency for Healthcare Research and Quality, U.S, Department of Health and Human Services
- CDC. US selected practice recommendations for contraceptive use 2013, 2° ed. Recommendations and Reports, vol. 62, n°5.
- CDC, US medical eligibility criteria for contraceptive uses . MMWR 2010; 59 (N°RR-4).
- Munro MG, Critchley HOD, Fraser IS, for the FIGO Menstrual Disorders Working Group. The FIGO classification of causes of abnormal uterine bleeding in the reproductive years. Fertil Steril 2011; 95(7):2204-2208.
- Fraser Ian. Introduction and summary of clinical data base. J Eur. Contraception and Health care 2008; 3(S1):1–3.
- Sociedad Argentina de Ginecología Infanto Juvenil. Ginecología infantojuvenil, un abordaje interdisciplinario. Ed. Journal, 2014. Cap. 4,9: 241.
- Emans. Laufer, Goldstein. “Ginecología en la infancia y la adolescencia” Ed Wolter Kluwer Health, S.A., Lippincott Williams &Wilkins, 2013. Cap 13: 138-271.
- Funk S, Miller MM, Mishell DR Jr, et al. Safety and efficacy of Implanon, a single-rod implantable contraceptive containing etonogestrel. Contraception. 2005; 71(5):319–326.
- Croxatto HB. Clinical profile of Implanon: a single-rod Etonogestrel contraceptive implant. Eur. J Contraception Reprod Health Care. 2000; 5 Suppl 2):21–28.
- Blumenthal P; Genzelli Danulson K et al. Tolerability and Clinical Safety of implanon. Eur. J of Contraception and reproductive health care. June 2008; 13(S1): 29-36.
- Aisen A.O; Enosolcase ME. Seguridad, eficacia y aceptabilidad de un anticonceptivo implantable de una sola varilla Etonorgestrel en la Universidad de Bening. J Clin Practice 2010; 13 (3):331-5.
- Noraziana A. Wahab, Nor Azlina A. Rahman, Kamarul B. Mustafa , Mokhtar Awang ,Ayu A. Sidek , Razman M. Ros . A clinical evaluation of bleeding patterns, adverse effects, and satisfaction with the subdermal etonogestrel implant among postpartum and non-postpartum users. International Federation of Gynecology and Obstetrics. Published by Elsevier Ireland Ltd 2016
- Obijuri L, MD; Bupus S, et al. “Etonorgestrel implants in adolescents: experience, satisfaction and continuation”. J. of Adolescent Health 58(2016) 284-289.
- Funks S; Miller mm; Mischel DR Jr, et al. La seguridad y eficacia de implanon, un anticonceptivo implantable de una sola varilla que contiene Etonogestrel. Anticoncepción mayo 2005; 71 (5): 319-2
- Guiahi ]M; Mc Bride M; Sheerder J et al. Short-term treatment of bothersome bleeding for Etonorgestrel implant user using a 14 days oral contraceptive pill regimen, a randomized controlled trial. Obstetric Gynecology 2015; 126:508-513.
- Katharine B Simmons, Alison B Edelmana, Rongwei Fub. “Tamoxifen for the treatment of breakthrough bleeding with the Etonogestrel implant: a randomized controlled trial”. http://dx.doi.org/10.1016/j.contraception.2016.10.001. 0010-7824/© 2016 Elsevier Inc.
- Hou M; McNichlas C and Creinm M. Combined oral contraceptive treatment for bleeding complain with the Etonorgestrel contraceptive implants: a randomized controlled trial. Eur J of Contraceptive and Rep Healthcare, 2016. Vol. 21, N°5: 361-366.
- Oneil-Callaham, Peper JF et al. “twenty four months continuation of reversible contraception”. Obstetric Gynecol 2013; 122:1083-91.
- Berlan E; Mizvaji K; Bonny A. “Twelve month discontinuation of Etonorgestrel implant in an outpatient pediatric setting”. Contraception 94(2016)81-86-
- Teunessin AM Grimm B. Continuation rates of the subdermal contraceptive Implanon R and associated influencing factor. Eur. J. Contracept Reproduct Health care 2014; 19:15-21.
- Peipert JF, Zhao W, et al. Continuation and Satisfaction of reversible contraception. JObstetric Gynecology 2011; 117:1105-13
- Hohmann H. Examiniting the efficacy, safety and patient acceptability of ETN implantable contraceptive. Patient Preference and adherence 2009¸3: 205-211
- Teunessin AM, Grimm B. Continuation rates of the subdermal contraceptive implanon and asociated influencing factor. Eur J Contracept Reprod Healthcare 2014; 19:15-21
- Lete Lasa Iñaki et al. “manejo clínico del sangrado producido con la utilización de métodos anticonceptivos con solo gestágenos”. Rev Iberoamericana de fertilidad y reproducción humana, 2011. Vol. 28- n°2 – ISSNN 1695-3705.
* Tocoginecóloga certificada en Ginecología Infanto Juvenil
Especialista en Endocrinología Ginecológica y Reproductiva
Jefa del Sector de Ginecología infanto Juvenil
Hospital de Niños “Dr. Orlando Alassia”, Santa Fe.
Mail: Esta dirección de correo electrónico está siendo protegida contra los robots de spam. Necesita tener JavaScript habilitado para poder verlo.