Avances en la Fisiopatología de la Endometriosis
Actualización • Dra. Elisabeth A. Domínguez *
RESUMEN
Este artículo trata sobre la actualización de los distintos mecanismos involucrados en el desarrollo, mantenimiento y progresión de la endometriosis.
ABSTRACT
This article deals with the updating of the different mechanisms involved in the development, maintenance and progression of endometriosis.
INTRODUCCIÓN
Se considera a la endometriosis una enfermedad de marcada dependencia hormonal (estrógeno-dependiente y progesterona-resistente) inflamatoria, con base genética (predisposición) y epigenética (interacción del medio ambiente), que involucran múltiples mecanismos moleculares, genéticos y celulares que han sido estudiados en esta última década, los cuales demuestran que se trata de una enfermedad crónica.
Distintos estudios tratan de explicar la fisiopatología, es decir, cómo llegan las células del endometrio al peritoneo, ovario, pero su desarrollo y progresión están ligados a las características del endometrio eutópico, como así también a la predisposición genética, desregulación hormonal e inmunovigilancia alterada.
FISIOPATOLOGÍA
La teoría de Sampson1 es la más aceptada; se trata de la llegada de las células endometriales a la cavidad pelviana a través del reflujo menstrual transtubárico. En el 90% de los casos, este tejido se destruye dado que presenta muerte celular programada (apoptosis), así como también un sistema inmunológico activo, pero en el 10% existe gran cantidad de factores involucrados, que desarrollaremos, y que favorecen el crecimiento de los focos endometriósicos.
Recientes publicaciones2 tratan de explicar formas de presentación antes de la menarca, en las cuales juegan un rol las stems cells y esto se relaciona con el sangrado uterino neonatal, el cual puede haber sido el flujo retrógrado inicial asociado a la presencia de estas células indiferenciadas, representando la fuente celular que llegarían a la cavidad peritoneal durante el período neonatal, convirtiéndose una endometriosis en la premenarca producto de la estimulación de la secreción de estrógenos prepúberes.
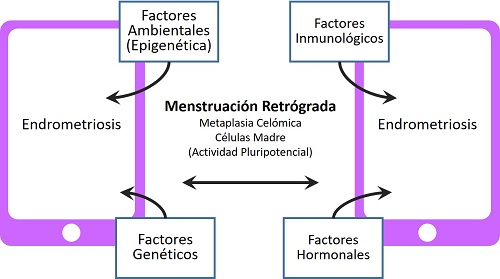
¿Cuáles serían los mecanismos involucrados en el desarrollo de la endometriosis? (Gráfico 1)
Desarrollaremos cada uno de ellos:
Gráfico 1: Mecanismos involucrados en el desarrollo de la endometriosis
Factores genéticos
La revolución genética cambió el foco de investigación de la endometriosis al permitir el estudio genómico y proteómico. El tejido del endometrio eutópico es el ideal para dichos estudios3.
Genética y endometrio
La biología del endometrio eutópico está ligada con el desarrollo de la endometriosis, ya que se encuentra una expresión anómala de genes, la cual genera la agresividad de este para el desarrollo y altera las isoformas del receptor de progesterona (isoforma A y B), lo que produce resistencia a esta última4.
El endometrio eutópico de estas pacientes contiene sustancias como la neurofilina I, que aumenta la producción de neuronas secretoras vinculadas al dolor, y las neurofilinas II, que aumentan la densidad de los vasos linfáticos, lo que contribuye a la difusión y autoperpetuación.
Otro aspecto es la mayor sobrevida del endometrio debido a resistencia al mecanismo de muerte celular programada (apoptosis) a causa de la sobreexpresión de la proteína BLC2 y al factor nuclear kappa beta5.
Otros aspectos para considerar son las evidencias científicas que han permitido asegurar que es una enfermedad poligénica (gran cantidad de genes desregulados). El trabajo colaborativo entre el Reino Unido y Australia6 estudió a 1100 familias en pacientes con 2 pares de hermanas con endometriosis y 1300 familias con 3 parientes afectados. Se observaron múltiples genes afectados y la región de mayor susceptibilidad fue para el cromosoma 7(p15) y 10(q26).
También existen polimorfismos genéticos que varían de acuerdo con la población y área geográfica, que intervienen en la expresión de proteínas que participan en procesos de angiogénesis, inmunológicos, etc.
Existe una predisposición familiar para las pacientes con familiares en primer grado (madre y hermana) de un riesgo 5 a 8 veces mayor de desarrollar la endometriosis7.
Factores ambientales
Elementos contaminantes (dioxinas) en conjunción con elementos dietarios (deficiencia de folatos) marcan la susceptibilidad para el desarrollo de esta enfermedad por medio de la disrupción de las funciones inmunológica y endocrina, considerándola así una enfermedad epigenética. Dicha interacción de toxinas o cambios en la alimentación, en determinado momento, pueden iniciar o generar progresión de la enfermedad8.
Los mecanismos de estos factores se traducen en la alteración de la función endocrina en el receptor de estrógenos, lo que provoca disrupción en su metabolismo y transporte sérico, como así también resistencia a la progesterona y cambios inmunológicos dado que la concentración de estrógenos genera mecanismos de inflamación con la participación del factor TNF-α, interleuquinas 1, 6, 8, 9.
Factores endocrinos
Hay 2 situaciones en relación con los estrógenos: por un lado, los polimorfismos de genes de la STAR (proteína reguladora de la esteroideogénesis) que producen mayor cantidad de estradiol, los cuales estimulan la vía de la prostaglandina E2 que en conjunto con las citoquinas (IL-1, 6, 8) darán inflamación y dolor. Otra situación está relacionada con los polimorfismos de genes de la actividad de la citocromo P450 aromatasa en el endometrio ectópico, esto genera grandes cantidades de estradiol estimulando la vía PGE2, F2 ALFA y Cox2, lo que provoca retroalimentación positiva sobre la aromatasa y el crecimiento del implante, inflamación y dolor9,10.
En conclusión, existen polimorfismos en los genes del endometrio eutópico que regulan la producción de estrógenos por medio de STAR y en el endometrio ectópico por medio de la citocromo P450 aromatasa; además en el endometrio eutópico existe resistencia a la progesterona con bajos niveles de esta hormona por alteración de las isoformas A y B del receptor.
Factores inmunológicos
Existe deficiencia en la inmunidad humoral demostrada por la presencia de anticuerpos y antígenos endometriales como depósito de complemento C3 en endometrio eutópico. Se asocia a otras enfermedades autoinmunes (tiroiditis, Crohn, artritis reumatoidea, LES, asma bronquial). Se debe tener en cuenta en los antecedentes familiares comparte con ellas la (base genética, el daño tisular y el déficit en linfocitos B y T)11,12.
Hay deficiencia en la inmunidad celular mediada por linfocitos natural killer (participan en la inmunovigilancia reconociendo y destruyendo las células), que se encuentran disminuidos en su función dentro del líquido peritoneal. También las proteínas ICAM favorecen que el tejido endometrial ectópico evada la inmunovigilancia y contribuyen a la adhesión celular del tejido al peritoneo pelviano.
Otro de los elementos involucrados es la aberración de los macrófagos (mayor cantidad y actividad), lo que conduce a mayor concentración de citoquinas y factores de crecimiento que generan inflamación y proliferación del implante, y sobrevida13-16.
Líquido peritoneal
Regula el ambiente peritoneal, estableciendo comunicación entre las células del sistema inmune. Se encuentra constituido por linfocitos y monocitos pero el 85% son macrófagos y, como dijimos antes, estos al estar alterados producen citoquinas y factores de crecimiento que regulan el desarrollo y la progresión del tejido ectópico endometrial.
Como dijimos, las citoquinas son las interleuquinas (IL-1, 6, 8) involucradas en el proceso inflamatorio crónico; los factores de crecimiento TNF-α participan en la adhesión del tejido (implantación); el factor de crecimiento neuronal provoca alta concentración de neuronas sensitivas relacionadas con el intenso dolor y el factor de crecimiento endotelial (VEGF) actúa formando vasos sanguíneos en el implante, es decir, neoangiogénesis mediante la cual el tejido sobrevive y crece17-20.
¿Cómo realiza el tejido endometrial ectópico el mecanismo de implantación?
- Debe adherirse.
- Degradar la MEC.
- Proliferar.
- Adaptarse al medio ambiente.
- Realizar angiogénesis para mantener el desarrollo y su autoperpetuación.
Para resumir y unir todos los conceptos que hemos visto:
Para realizar la invasión peritoneal las células deben escapar al sistema de inmunovigilancia y adherirse a las células del peritoneo; aquí participan las fibronectinas que regulan la unión con la matriz extracelular, controlada por las metaloproteinasas (MMP), que al estar sobreexpresadas, la degradan potenciando la invasión. Participan el FNT-α y las proteínas ICAM. De esta manera invade y luego prolifera por todos los mecanismos que ya hemos expuesto para mantenerse y sobrevivir por medio de angiogénesis.
CONCLUSIONES
Podemos decir que no es suficiente que el tejido endometrial llegue a la cavidad pelviana a través del reflujo menstrual retrógrado. Debe sumarse a esto la alteración del complejo mecanismo de depuración de la sangre menstrual regulado por factores genéticos, del medio ambiente e inmunológicos, estos últimos íntimamente ligados a factores psíquicos y endocrinos. Se debe evaluar a las pacientes con un enfoque integral.
REFERENCIAS
- Sampson JA. Peritoneal endometriosis due to menstrual dissemination of endometrial tissue into the peritoneal cavity. Am J Obstet Gynecol 1927; 14:442-69.
- Brosens I, Benagiano G. Is neonatal uterine bleeding involved in the pathogenesis of endometriosis as a source of stem cells? Hum Reprod 2013 Nov; 28(11):2893-7.
- Wu Y, Strawn E, Basir Z, Wang Y, Halverson G, Jailwala P y cols. Genomic alterations in ectopic and eutopic endometria of women with endometriosis. Gynecol Obstet Invest 2006; 62:148-5.
- Aghajanova L, Velarde M, Giudice LC. Progesterone receptor. Endocrinologia 2009; 150:3863-3870.
- Gilabert Estellés J. Nuevas perspectivas en la endometriosis. Desde la fisiopatología al tratamiento médico de la enfermedad. Revista Iberoamericana de Fertilidad y Esterilidad 2011 Mar; 28(1).
- Treloar S, Kennedy S. (FALTA TÍTULO DEL TRABAJO) Am J Hum Genet 2005; 77:365.
- Simpson JL, Elias S, Malinak LR, Buttram VC Jr. Heritable aspects of endometriosis. I. Genetic studies. Am J Obstet Gynecol 1980; 137:327-31.
- Szczepanska M, Mostowska A, Wirstlein P. Polymorphic variants of folate and choline metabolism genes and the risk of endometriosis. Eur J Obstet Gynecol Reprod Biol 2011 Jul; 157(1):67-72.
- Izawa M, Taniguchi F. Epigenetic aberration of gene expression endometriosis. Front Biosci (Elite Ed) 2013 Jun 1; 5:900-10.
- Schenken RS. Menstrual endometrial cells from women with endometriosis demonstrate increased adherence to peritoneal cells and increased expression of CD44 splice variants. Fertil Steril 2010; 93:1745-1749.
- Eisenberg VH, Zolti M, Soriano D. Is there an association between autoimmunity and endometriosis? Autoimmun Rev 2012 Sep; 11(11):806-14.
- Nowak NM, Fischer OM, Gust TC, Fuhrmann U, Habenicht UF, Schmidt A. Intraperitoneal inflammation decreases endometriosis in a mouse model. Hum Reprod 2008; 23:2466-74.
- Berbic M, Schulke L, Markham R, Tokushige N, Russell P, Fraser IS. Macrophage expression in endometrium of women with and without endometriosis. Hum Reprod 2009; 24:325-32.
- Matarese G, De Placido G, Nikas Y, Alviggi C. Pathogenesis of endometriosis: natural immunity dysfunction or autoimmune disease? Trends Mol Med 2003; 9:223-28.
- Fuji EY, Nakayama M, Nakagawa A. Concentrations of receptor for advanced glycation end products, VEGF and CMLin plasma, follicular fluid, and peritoneal fluid in women with and without endometriosis. Reprod Sci 2008; 15:1066-1074.
- Khan KN, Kitajima M, Hiraki K, Fujishita A, Sekine I, Ishimaru T, Masuzaki H. Immunopathogenesis of pelvic endometriosis: role of hepatocyte growth factor, macrophages and ovarian steroids. Am J Reprod Immunol 2008; 60:383.
- Gonzalez Ramos R, Van Langendonckt A, Defrere S, Lousse JC, Colette S, De voto L y cols. Involvement of the nuclear factor-kappaB pathway in the pathogenesis of endometriosis. Fertil Steril 2010; 94:1985-94.
- Burney R, Giudice L. Pathogenesis and pathophysiology of endometriosis. Fertil Steril 2012; 98:511-519.
- Krikun G. Endometriosis, Angiogenesis and Tissue Factor. Scientifica 2012; 2012:306830.
- Méndez Ribas JM y cols. Enfoque actual de la adolescente por el ginecólogo (3ª edición), Cap. 29. Buenos Aires: Editorial Ascune Hnos. 2015:250-257.
* Especialista en Ginecología. Especialista en Ginecología Infantojuvenil
Miembro de la CD de SAGIJ
Coordinadora General del Programa de Adolescencia, Hospital de Clínicas José de San Martín
Esta dirección de correo electrónico está siendo protegida contra los robots de spam. Necesita tener JavaScript habilitado para poder verlo.

